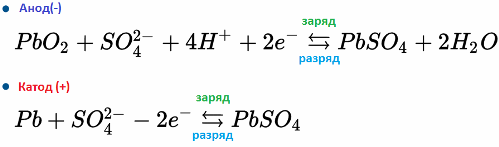luokat: Kuinka se toimii?, Auto-sähköasentaja
Katselukuvien lukumäärä: 16526
Kommentit artikkeliin: 0
Laite ja akun toiminnan periaate
Sähköakkua kutsutaan uudelleenkäytettävä kemiallinen virtalähde. Akun sisällä olevat kemialliset prosessit, toisin kuin kertakäyttöisissä galvaanisissa kennoissa, kuten alkali- tai suolaakkuissa, ovat palautuvia. Sähköenergian varauksen purku-, kertymis- ja palautussyklit voidaan toistaa useita kertoja.
Joten akun toimintaperiaate antaa sinun käyttää sitä syklisesti useiden laitteiden, kannettavien laitteiden, ajoneuvojen, lääkinnällisten laitteiden jne. Autonomiseen virtalähteeseen täysin eri alueilla.

Puhuessaan sanaa "akku", he tarkoittavat joko itse akkua tai akkukennoa. Useat sarjaan tai rinnan kytketyt toisiinsa paristokennot muodostavat pariston, samoin kuin useita liitettyjä paristoja.
Ensimmäinen paristo, toisin sanoen uudelleenkäytettävä galvaaninen kenno, ilmestyi virallisten lukujen mukaan vuonna 1803. Sen on luonut saksalainen fyysikko ja kemisti Johann Wilhelm Ritter. Oerstedin ystävä Ritter, joka ei ole tutkija, tutki valon kemiallisia vaikutuksia, teki kokeita elektrolyysillä, muuten, hän kuuluu sähkömagneettisen spektrin ultraviolettiosan löytämiseen.
Tutkiessaan voltaattista pylvästä Ritter otti viisikymmentä ympyrää kuparia, märän kankaan paloja ja muodosti kolmenkymmenenkymmenen tällaisen ympyrän ja märän kankaan kolonnin niiden väliin. Ohjaten virtaan voltaattikolonnista rakenteen läpi, Ritter huomasi, että navansa oli varautunut ja siitä itsestään tuli sähkön lähde. Tämä oli ensimmäinen akku.
Kemiallisen reaktion palautuvuus elektrolyytissä ja akun elektrodeissa antaa sinun palauttaa akun työkyky - ladata se purkamisen jälkeen. Virta latauksen aikana johdetaan akun läpi vastakkaiseen suuntaan purkautumiseen nähden.
Esimerkiksi lyijyakku toimii lyijyn ja rikkihappossa olevan lyijydioksidin sähkökemiallisten reaktioiden vuoksi. Alla olevat kaavat heijastavat anodissa ja katodissa tapahtuvia palautuvia reaktioita: vasemmalta oikealle - reaktio purkamisen aikana, oikealta vasemmalle - varaus.
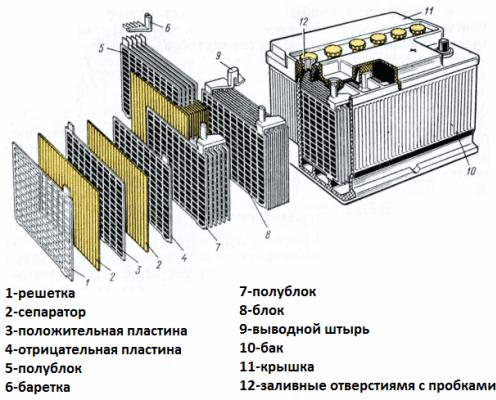
Tarkastele nyt akkulaitetta esimerkkinä auton käynnistysakusta. Sen jännite on 12 volttia. Akku koostuu kuudesta solusta, jotka on kytketty sarjaan, erotettuna osioilla.
Sarjayhteys tarkoittaa tässä tapauksessa, että yhden solun negatiivinen napa on kytketty seuraavan solun positiiviseen napaan.
Jokainen elementti sisältää parin hilaelektrodia lyijy-antimoniseoksesta upotettuna elektrolyyttiin, joka on rikkihapon 38-prosenttinen vesiliuos. Huokoinen erotin eristää elektrodit toisistaan estäen oikosulkujen välillä, mutta kulkee elektrolyytin vapaasti itsensä läpi. Toisin sanoen neste täyttää sekä lyijylevyjen solut että erottimien huokoset.
Saman nimiset levyt on kytketty toisiinsa lyijyhyppylaitteilla, samoin kuin levypaketit, jotka on erotettu väliseinillä, jotka muodostavat yksittäiset elementit, ja akun navat ovat myös lyijyä.
Auton akun päätelmät eroavat toisistaan aina hiukan hiukan toisistaan - positiivisen navan halkaisija on suurempi kuin negatiivisen, jotta kytkettäessä ei tehdä virhettä.
Akkurasia on valmistettu dielektrisestä materiaalista, joka kestää aggressiivisia ympäristöjä, äärimmäisiä lämpötiloja ja tärinää. Nykyään käynnistysakkujen kotelot on valmistettu polypropeenista.
Kotelo on ilmatiiviisti suljettu kansi, varustettu laipoilla kestävää kiinnitystä varten.Vanhojen paristojen tapauksessa jokaiselle akun muodostavalle galvaaniselle kennolle on aina järjestetty pistotulppa, jotta tarvittaessa voidaan lisätä tislattua vettä. Moderneissa huoltovapaissa akkutulpissa tapauksissa ei ole.
Muut artikkelit paristoista ja niiden käytöstä:
Kuinka aurinkovoimalaitosten akut ovat?
Katso myös osoitteesta electro-fi.tomathouse.com
: